Une nouvelle publication en collaboration dans "Science" pour l'Equipe DO-IT
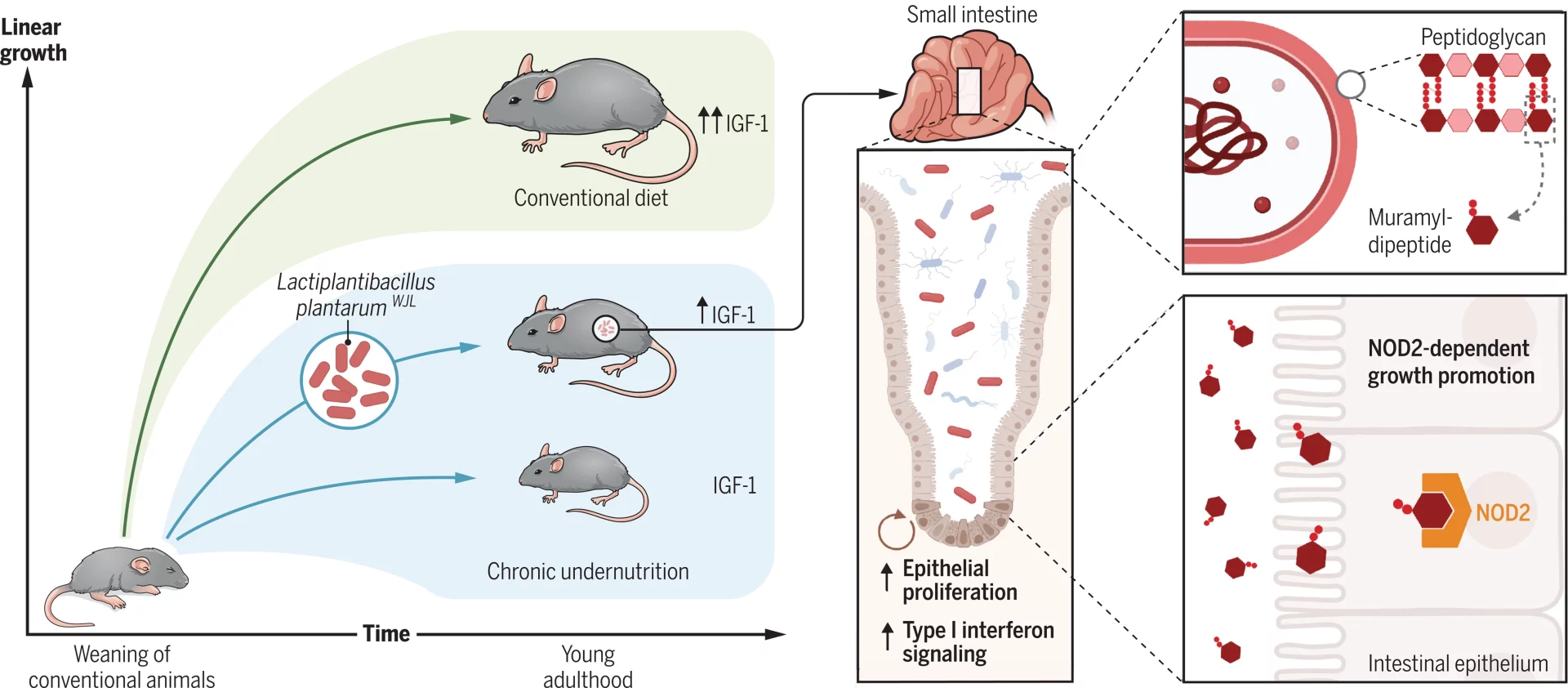
Le microbiote intestinal est aujourd’hui considéré comme un organe à part entière. Une équipe pilotée par des scientifiques du CNRS et de l’ENS de Lyon, en collaboration avec l’Université Claude Bernard Lyon 1, l’Inserm, et l’Inrae a travaillé sur ce sujet dans une publication à paraître dans la revue Science. Les scientifiques ont découvert, chez l’animal, comment une bactérie du microbiote pouvait stimuler la croissance juvénile dans des conditions nutritionnelles appauvries.
L’activité du microbiote est essentielle à une vie en bonne santé mais elle reste encore mal comprise. Dans de précédentes études, l’équipe de recherche avait révélé que le microbiote intestinal joue un rôle important dans la croissance des jeunes individus chez des espèces aussi distantes que l’insecte drosophile ou la souris domestique.
En particulier, une souche de la bactérie Lactiplantibacillus plantarum (LpWJL) est particulièrement efficace pour stimuler la croissance juvénile de ces animaux dans des conditions nutritionnelles appauvries. Dans cette nouvelle étude, l’équipe de recherche internationale1 dirigée par des scientifiques de l’Institut de génomique fonctionnelle de Lyon (CNRS/ENS de Lyon) a identifié l’un des mécanismes par lequel cette bactérie agit sur la croissance de souriceaux en sous-nutrition après le sevrage2 .
L’administration quotidienne par voie orale de la bactérie LpWJL à ces souriceaux stimule localement la maturation de l’épithélium intestinal ce qui soutient la production d’hormones (insuline et IGF-13 ) essentielles à une croissance saine. Les scientifiques ont identifié une molécule produite par la bactérie et un composant majeur des parois cellulaires bactériennes : le muramyldipeptide. Cette molécule est suffisante pour stimuler la production d’insuline et d’IGF-1 en se fixant à NOD2, un récepteur présent sur les cellules de l’épithélium intestinal chez la souris.
Ces résultats établissent que le muramyldipeptide et son récepteur NOD2 contribuent à atténuer des retards de croissance liés à une sous-nutrition chronique. Ces travaux permettent d’envisager chez les enfants en sous-nutrition chronique des interventions bactériennes couplées à des interventions nutritionnelles afin d’améliorer leur dynamique de reprise de croissance. Enfin ils offrent aussi des perspectives d’études sur d’autres populations nécessitant une nutrition optimisée telle que les personnes âgées ou les sportifs de haut-niveau.
© Amélie Joly
Bibliographie
Microbe-mediated intestinal NOD2 stimulation improves linear growth of undernourished infant mice. Martin Schwarzer, Umesh Kumar Gautam, Kassem Makki, Anne Lambert, Tomas Brabec, Amelie Joly, Dagmar Šrůtková, Pierre Poinsot, Tereza Novotná, Stéphanie Geoffroy, Pascal Courtin, Petra Petr Hermanová, Renata C. Matos, Jonathan J.M. Landry, Céline Gérard, Anne-Laure Bulteau, Tomáš Hudcovic, Hana Kozaková, Dominik Filipp, Marie-Pierre Chapot-Chartier, Marek Šinkora, Noël Peretti, Ivo Gomperts Boneca, Mathias Chamaillard, Hubert Vidal, Filipe De Vadder, François Leulier, Science, 24 février 2023. – DOI : www.science.org/doi/10.1126/science.ade9767
Contact
Notes
- En France, ont également participé des scientifiques du laboratoire Microbiologie intégrative et moléculaire (CNRS/Institut Pasteur), de l’Institut Micalis (Inrae/Agroparistech/Université Paris-Saclay), du laboratoire Physiologie cellulaire (Inserm/Université de Lille), du laboratoire Carmen (Inserm/Inrae/ Université Lyon Claude Bernard Lyon 1), du Service de gastroentérologie, hépatologie et nutrition pédiatriques des Hospices civils de Lyon. A l’étranger, ces recherches ont impliqué des scientifiques de l’Académie des sciences de République tchèque et de l’European Molecular Biology Laboratory (Allemagne).
- Phase de développement post-natal correspondant à la fin de l’alimentation par le lait maternel et au début de l’alimentation autonome.
- Le facteur de croissance IGF-1 (Insulin-like Growth Factor 1), produit principalement par le foie, présente une structure chimique proche de celle de l’insuline mais des fonctions distinctes. L’IGF-1 stimule la croissance tissulaire et squelettique et l’insuline régule le métabolisme énergétique nécessaire à la croissance.

