Depuis sa création, le CRNH est fonctionnellement organisé en 2 plateformes : une plateforme de recherche clinique permettant l’investigation sur volontaires sains et patients, localisée dans le bâtiment CENS-ELI 2D, et une plateforme analytique de spectrométrie de masse dans le bâtiment CBPS 3D, au Centre Hospitalier Lyon Sud situé à Oullins/Pierre Bénite.

Centre de Recherche en Nutrition Humaine - Rhône-Alpes

Plateforme CRNH-RA

La Plateforme CRNH-RA de recherche clinique en nutrition a pour objet de fournir à l’ensemble de la communauté académique locale, nationale et internationale mais aussi au monde socio-économique une infrastructure spécifiquement dédiée à l’exploration clinique dans le domaine de la nutrition humaine.
L’expertise de la plateforme porte plus particulièrement sur :
- Le rôle de la phase postprandiale dans les effets de l’alimentation
- Les mécanismes d’adaptations nutritionnelles : stress métabolique et environnement
- La modulation de la qualité nutritionnelle de l’alimentation
- Le rôle du microbiote intestinal sur le métabolisme
- L’impact de la chirurgie bariatrique
- L’étude de la sensibilité à l’insuline (clamp) et de la dépense énergétique
- Le comportement alimentaire et l’analyse sensorielle
Pour toutes propositions de collaboration sur des projets de recherche, contactez-nous

Les services proposés par la plateforme CRNH-RA sont:
- La conception et la rédaction de protocoles de recherche,
- Soutenir ou participer à des protocoles aux instances réglementaires (comité d’éthique, agence nationale de sécurité du médicament et des produits de santé, Commission nationale de l’informatique et des libertés)
- Le recrutement de volontaires
- La réalisation du protocole, dont l’accueil de volontaires pour des explorations cliniques
- La gestion des actes médicaux ou paramédicaux,
- Le suivi des protocoles et l’accueil d’audits,
- L’analyse des résultats,
- La préparation des rapports d’étude et la valorisation des résultats (publications, communications, brevets…).

Les principales explorations cliniques réalisées sont :
- La composition corporelle (impédancemétrie, Bodpod, DEXA, IRM, eau doublement marquée)
- Le métabolisme énergétique (calorimétrie indirecte, eau doublement marquée)
- La sensibilité à l’insuline (clamp euglycémique hyperinsulinique)
- La biodisponibilité et devenir des aliments/substrats via la perfusion/ingestion de traceurs isotopiques stables
- Les challenges nutritionnels (repas tests, métabolisme postprandial, …)
- Le comportement alimentaire et la micro-structure du repas via un buffet standardisé
- Les métabolismes glucidique, lipidique, lipoprotéines
- Les profils hormonaux
- Les paramètres inflammatoires et stress oxydant, et marqueurs de risque cardio-vasculaire et de fonction endothéliale
- Le métabolisme hépatique
- La composition et fonctionnalité du microbiote intestinal (incluant AGCC, acides biliaires, gaz expirés…)
- Les échantillons biologiques prélevés : sang, plasma, sérum, urines, selles, tissu adipeux, tissu musculaire, salive, gaz expirés
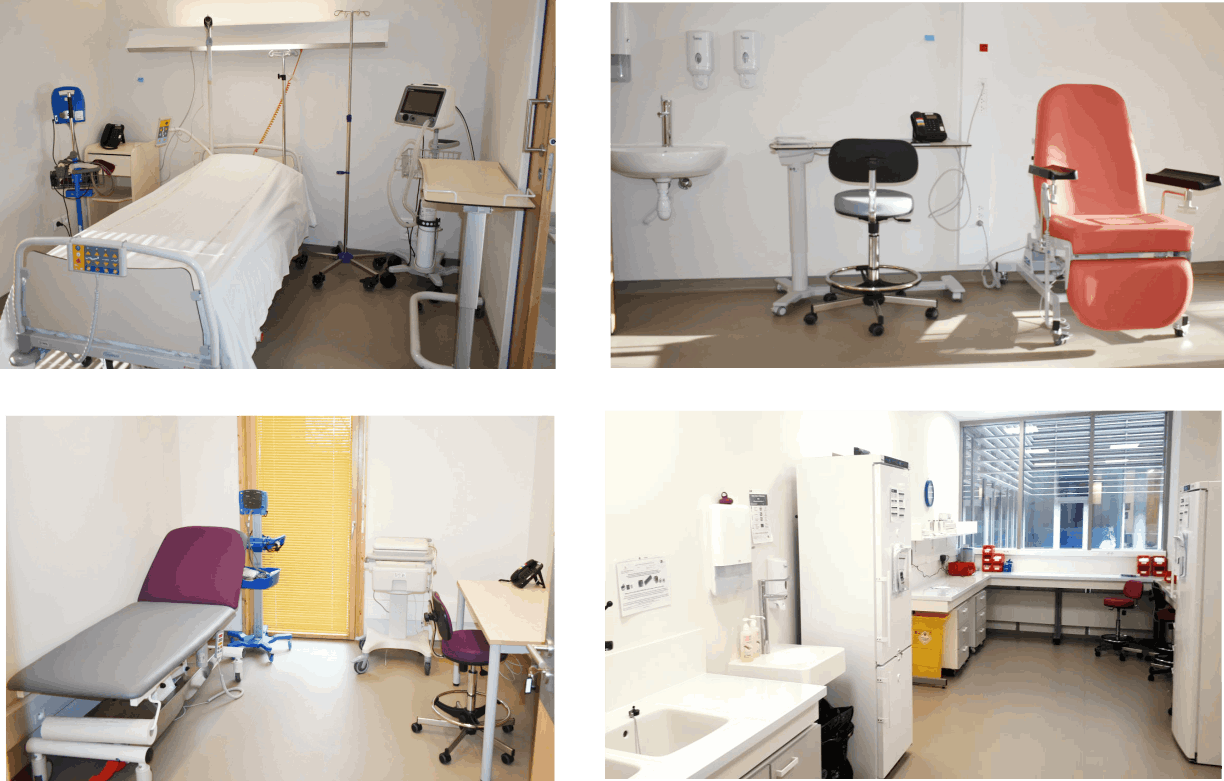
Une infrastructure adaptée au sein du bâtiment CENS-ELI
(financée par le programme IRN-CENS de la région AURA et l’Université Claude Bernard Lyon1)
qui est composée des pièces dédiées à l’exploration clinique chacune équipée de matériels spécifiques à la recherche en nutrition :
- 2 Chambres test de jour
- 3 Chambres hébergement avec salle de bain
- 3 box d’examen
- 1 Pièce test avec 4 fauteuils de prélèvements
- 1 Salle de prélèvements avec 1 fauteuil
- 2 Laboratoires de conditionnement
- 1 Box de test (EEG et Bodpod)
- 1 Restaurant expérimental et cuisine
- 1 Salle de gym
- 1 Studio d’enregistrement

Une équipe de recherche spécialisée,
Avec du personnel médical et paramédical formé à la nutrition et à la recherche clinique (médecin investigateur, infirmier de recherche clinique, diététicienne, attaché de recherche clinique…).
Autorisation de lieu de recherches :
Arrêté n°2019-17-0582 portant autorisation de lieu de recherches impliquant la personne humaine SANS première administration à l’homme d’un médicament, valable jusqu’au 07/10/2026.
Pour toute demande, vous pouvez contacter la coordinatrice scientifique
Plateforme Metanutribiota

La plateforme Metanutribiota est une plateforme d’analyse métabolomique spécialisée dans le dosage et la caractérisation de molécules biologiques issues ou associées à la nutrition et aux microbiotes.
Elle rassemble les moyens techniques requis pour la réalisation de projets métabolomiques, depuis l’extraction des métabolites de la matrice biologique en passant par leur analyse sur des équipements de spectrométrie de masse spécifiques et jusqu’au rendu des résultats.
L’expertise historique de la plateforme est de réaliser des mesures d’enrichissements isotopiques sur des échantillons prélevés au cours de protocoles cliniques chez l’homme, sur des modèles animaux ou cellulaires utilisant des isotopes stables. Le laboratoire réalise également la quantification de métabolites variés (lipides, glucides, acides aminés) et certains métabolites produits par le microbiote intestinal dont les AGCC.
Les thématiques analytiques du centre d’analyse sont :
- La biodisponibilité des aliments, devenir des substrats et flux métaboliques
- Les lipides, glucides, acides aminés et métabolites du microbiote intestinal
- La composition corporelle et dépense énergétique totale (eau doublement marquée)
- La sensibilité à l’insuline (clamp euglycémique hyperinsulinique)
- La volatolomique des gaz expirés
- La métabolomique ciblée et multi ciblée
Pour toute demande, vous pouvez contacter le(s) responsable(s) de la plateforme Metanutribiota.

Equipements

Spectromètre de masse isotopique avec plusieurs couplages disponibles :
- GC-Combustion & GC-pyrolyse
- Thermal Conversion Elemental Analysis
- Breath tests

Spectromètre de masse organique
Spectromètre de masse organique couplé à un chromatographe en phase gazeuse disposant d’un système d’injection multimodes comprenant la micro-extraction sur phase solide (SPME, Gerstel & CTC Analytics).
3 modes d’ionisation disponibles :
- Ionisation par impact électronique
- Ionisation chimique positive
- Ionisation chimique négative

TD-GC/MS
Spectromètre de masse organique couplé à un chromatographe en phase gazeuse, disposant d’une interface de thermo-désorption avec un système d’injection multimodes comprenant la micro-extraction sur phase solide.

LC-MS/MS
Système ACQUITY UPLC PREMIER / Xevo TQ-XS (Waters) : système UPLC couplé à un spectromètre de masse de type triple quadripole. Ce système permet le développement de méthodes d’analyse « in house » ciblées et est compatible avec les kits de métabolomique et lipidomique multiciblée de la société Biocrates.
Analyses proposées
Biodisponibilité des aliments et Flux métaboliques
Glucides, Lipides et Acides aminés marqués au 2H ou 13C :
- Glucides (plasma)
- Lipides (plasma, selles, tissus, milieu cellulaire)
- Acides aminés (plasma)
Microbiote intestinal
- Acides gras à chaîne courte (AGCC) : 13C et concentrations (plasma, selles, milieu cellulaire)
- Composés organiques volatiles COV (gaz expirés)
- Acides biliaires
- Métabolomique et lipidomique multi-ciblée (Kit MxP 500 Quant (XL) Biocrates) : environ 1000 métabolites et 39 classes biochimiques (sérum/plasma/urines/fèces)
Sensibilité à l’insuline
Clamp euglycémique hyperinsulinémique avec [6,6-2H2] glucose
Oxydation des substrats
- 13CO2 Breath test (molécules marquées au 13C)
- 2H urinaire (molécules marquées au 2H)
Composition corporelle
Eau marquée 2H2O ou H218O :
2H ou 18O (urines, salive ou plasma)
Dépense énergétique totale
Eau doublement marquée 2H218O :
2H ou 18O (urines, salive ou plasma)

